항생제 종류 및 개요
항생제 종류
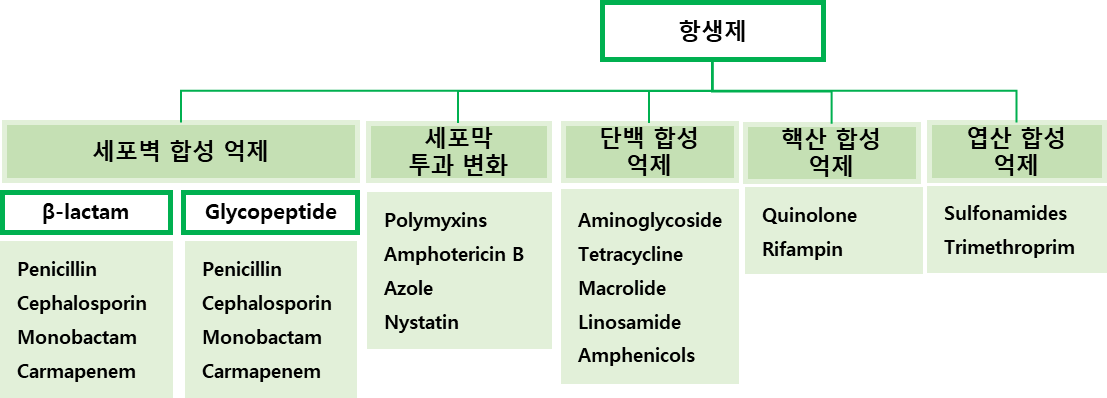
1. 세포벽 합성 억제 (Cell Wall Synthesis Inhibitors)
β-Lactam계: Penicillins, Cephalosporins, Carbapenems, Monobactams
작용 기전: PBP(Penicillin-Binding Protein) 결합 및 세포벽 교차 결합(cross-linking) 차단
Glycopeptides: Vancomycin, Teicoplanin (Gram(+)에만 작용)
작용 기전: D-Ala-D-Ala 말단에 결합하여 중합 차단
Siderophore Cephalosporins: Cefiderocol
특징: 세균의 철분 흡수 경로(Iron uptake pathway)를 이용해 세포 내로 진입 후 PBP3 억제
Lipoglycopeptides: Dalbavancin, Oritavancin
기타: Fosfomycin (MurA 억제), Bacitracin (지질 운반체 억제)
2. 단백 합성 억제 (Protein Synthesis Inhibitors)
30S Ribosome 억제
Aminoglycosides (살균): Gentamicin, Tobramycin, Amikacin
Tetracyclines (정균): Doxycycline, Minocycline, Tigecycline
50S Ribosome 억제
Macrolides: Azithromycin, Clarithromycin
Lincosamides: Clindamycin
Oxazolidinones: Linezolid, Tedizolid (개시 복합체 형성 억제)
Pleuromutilins: Lefamulin (Peptidyl transferase center 결합)
Chloramphenicol, Streptogramins (Quinupristin/Dalfopristin)
tRNA Synthetase 억제: Mupirocin (Isoleucyl tRNA synthetase 억제)
3. 핵산 합성 억제 (Nucleic Acid Synthesis Inhibitors)
DNA Gyrase / Topoisomerase IV 억제: Fluoroquinolones (Ciprofloxacin, Levofloxacin)
RNA Polymerase 억제: Rifampin
DNA 손상 (Free radical 생성): Metronidazole, Nitrofurantoin
4. 대사 억제 (Folate Antagonists)
Dihydrofolate reductase (DHFR) 억제: Trimethoprim
Dihydropteroate synthase (DHPS) 억제: Sulfonamides
병용 요법: TMP-SMX (Trimethoprim-Sulfamethoxazole)
5. 세포막 기능 억제 (Cell Membrane Disruptors)
Polymyxins: Colistin, Polymyxin B (LPS에 결합하여 외막/내막 붕괴)
Lipopeptides: Daptomycin (Gram(+) 세포막 전위차 파괴)
[1] Harrison 22e, Chap 149
항생제 내성균의 계보 및 다재내성균
1. 주요 항생제 내성 기전 (Mechanisms of Resistance) - 참고
약물 유입 감소 (Decreased Permeability)
Loss of porins: Carbapenems (Imipenem 등) 내성 (주로 P. aeruginosa, Enterobacteriaceae)
Altered iron uptake pathways: Cefiderocol 내성 (철분 운반체 변이)
약물 배출 펌프 과발현 (Efflux Pump Overexpression)
Quinolones, Tetracyclines (Tigecycline), Chloramphenicol 배출
β-lactams (Meropenem): 그람음성균에서 배출 펌프를 통한 내성
Aminoglycosides: 능동적 배출로 인한 내성
타겟 변형 (Target Modification)
Ribosomal mutation/modification:
Tetracyclines: 30S 리보솜 보호 단백질 또는 결합 부위 변형
Oxazolidinones (Linezolid): 23S rRNA 변이 또는 메틸화(cfr gene)
Lefamulin: 50S 리보솜 결합 부위 변형 (TetM or TetO)
Aminoglycosides: 16S rRNA methylation (고도 내성 유발)
Target mutations (DNA gyrase/Topoisomerase IV): Quinolones 내성
Lipopolysaccharide (LPS) structure mutation: Polymyxin (Colistin) 내성 (전하 변경으로 결합 방해)
효소에 의한 불활성화 (Enzymatic Inactivation)
β-lactamases in periplasmic space: β-lactams 분해 (ESBL, Carbapenemase 등)
Antibiotic-modifying enzymes: Aminoglycosides (Acetyl/Adenyl/Phospho-transferase), Ciprofloxacin (일부 효소에 의한 변형)
대사 경로 우회 (Bypass Targets)
Trimethoprim: 내성 Dihydrofolate reductase 생성
Sulfonamides: 내성 Dihydropteroate synthase 생성
유전적 요소 (Genetic Elements)
Plasmid: 항생제 내성 유전자(β-lactamase 등)를 담아 균주 간 전파
2. 주요 내성균의 치료 흐름 (Clinical Progression) - 반드시 암기
S. aureus
Penicillin (대부분 내성) → Methicillin/Oxacillin (MSSA) → Vancomycin / Linezolid / Daptomycin / Ceftaroline (MRSA)
Enterococcus
Ampicillin → Vancomycin → Linezolid / Daptomycin (VRE)
Enterobacteriaceae (E. coli, Klebsiella)
3세대 Cephalosporin 내성 (ESBL) → Carbapenem 사용
Carbapenem 내성 (CRE) → Ceftazidime-avibactam, Meropenem-vaborbactam, Cefiderocol, Colistin 등 사용
Pseudomonas / Acinetobacter
Piperacillin-tazobactam / Ceftazidime / Cefepime / Carbapenem 내성 시 → Ceftolozane-tazobactam, Cefiderocol, Colistin 등 고려
[1] Harrison 22e, Chap 150
항생제 내성검사의 해석
항생제 내성 검사 (Antimicrobiogram) 의 예시 및 해석
Case 1
S.aureus 확인
항생제 내성의 계보 순서대로 항생제 별 내성 확인
Penicillin 내성
Oxacillin 내성
Vancomycin 감수성
MRSA 에 해당 → Vancomycin 선택
Case 2
K. pneumonia 확인
항생제 내성의 계보 순서대로 항생제 별 내성 확인
Cephalosporin: 감수성 / ESBL negative
Carbapenem: 감수성
감수성 있는 항균제 중 가장 narrow spectrum 을 사용 → ceftriaxone/cefotaxime 우선 선택
Case 3
K. pneumonia 확인
항생제 내성의 계보 순서대로 항생제 별 내성 확인
Cephalosporin: 내성
Carbapenem: 내성
Colistin: 감수성
CRE (Carbapenem resistant enterobacteriaceae) 확인 → colistin 선택
향균력의 구분 및 약물농도모니터링 (Therapeutic Drug Monitoring, TDM)
농도 의존성 항생제 (Concentration-dependent killing)
특징: 혈중 최고 농도(Cmax)가 높을수록 살균력이 증가함. Cmax/MIC 비율이 중요.
Post-antibiotic effect (PAE): 농도가 MIC 미만으로 떨어져도 세균 억제 효과가 지속됨 → 하루 1회 고용량 투여 가능
주요 약물: Aminoglycosides, Fluoroquinolones (AUC/MIC), Daptomycin, Metronidazole
시간 의존성 항생제 (Time-dependent killing)
특징: 농도가 최소 억제 농도(MIC)보다 높은 상태로 유지되는 시간(T > MIC)이 중요함
투여 전략: 1회 용량을 늘리는 것보다 투여 횟수를 늘리거나 지속 주입(Continuous infusion)하는 것이 유리함
주요 약물: β-Lactams (Penicillins, Cephalosporins, Carbapenems), Macrolides (Erythromycin 등 일부)
AUC/MIC 의존성 (시간-농도 복합 의존)
특징: 24시간 동안의 약물 노출 총량(Area Under Curve)이 중요함.
주요 약물: Vancomycin, Fluoroquinolones, Tetracyclines, Linezolid
TDM (Therapeutic Drug Monitoring)
항생제 사용 시 치료 범위(Therapeutic window)가 좁아 독성 위험이 있거나 효과를 정밀하게 조절해야 할 때 시행
주로 Aminoglycoside 계열과 Glycopeptide 계열이 대표
Aminoglycoside 계열: 농도 의존적(Concentration-dependent) 살균 작용을 하며, 신독성과 이독성(귀 독성) 부작용이 있어 TDM이 필수적
해당 약물: Amikacin, Gentamicin, Tobramycin
측정 시점:
Peak (최고 농도): 투여 종료 후 약 30분~1시간 뒤 측정. 충분한 살균 효과를 얻기 위한 목표치에 도달했는지 확인
Trough (최저 농도): 다음 차례 투여 직전(30분 전)에 측정. 약물이 체내에서 충분히 배설되었는지 확인하여 독성(특히 신장 축적)을 예방
Glycopeptide 계열: 시간 의존적(Time-dependent) 살균 작용을 하며, 최근 지침에 따라 측정 방식에 변화가 있음
해당 약물: Vancomycin, Teicoplanin
측정 시점:
Trough (최저 농도): 보통 Trough 위주로 관리. 혈중 농도가 일정 수준 이상 유지되어야 내성을 방지하고 효과를 볼 수 있기 때문입니다. (보통 4회차 투여 직전에 측정)
Peak (최고 농도): 일반적으로는 잘 측정하지 않으나, 투과력이 떨어지는 부위(뇌수막염 등)의 감염이거나 신기능이 극도로 불안정한 경우 예외적으로 측정
참고: 최근 Vancomycin의 경우, 단순 Trough 농도보다는 AUC/MIC(24시간 농도 곡선 하 면적 대비 최소 억제 농도) 비율을 400~600으로 유지하는 것을 권장하며, 이를 위해 정교한 계산법을 사용
[1] Harrison 22e, Chap 149
연습문제 11문제
0/11 완료
0개의 글
** 제목만 보더라도 어떤 내용인지 알 수 있도록 완성된 문장으로 작성해주세요.
예시) 초음파 (X) → 초음파 사진에서 PDA 소견을 어떻게 알 수 있나요? (O)


